切迫早産について
正期産以前(妊娠22週0日~36週6日)の分娩を「早期産(早産)」といい、早産が起こるような一歩前の状態を「切迫早産」という。今日では、子宮頚管の炎症反応とそれが波及した絨毛羊膜炎が原因といわれており、放置しておくと破水したりする可能性もある。なお、早産週数によって児の予後も大きく左右するので、児にとって少しでも成熟した状態で出生することが望まれる。ただし、そのような状態で長く母体の子宮内に留まるということは、感染を含めた悪い環境に児が接する可能性もあり、分娩のタイミングを見逃さないことも大切である。
第1回目の妊娠合併症が第2回目の妊娠で反復する可能性について:
Obstet.Gynecol.2009;113:1217に1978-2007年までの間にデンマークで行われた536419例のcohort研究の結果が報じられている。
第1回目の妊娠と比べて第2回目の妊娠では:
① 32-36週での早産は2.7%から14.7%へと6.12倍に増加
② 28週未満の早産は、第2回目の妊娠で26%と著増
③ 32―36週での妊娠高血圧の合併は14.1%から25.3%に2.08倍の増加
④ LFDの割合は3.1%から9.6%に2.82倍に増加
⑤ 胎児発育が標準よりも2-3SD以下のケースが1.1%から1.8%と1.62倍に増加
すなわち、早産・妊娠高血圧・胎児発育の障害が高率に反復することが判明したとしている。
当院における「切迫早産」の管理について
(1) 「切迫早産」の診断(補助診断も含む)
A 問診(腹緊・腹痛の自覚など)
B 内診(子宮口の開きぐあいや展退、軟らかさなど)
C 子宮頚管粘液中顆粒球エラスターゼ(絨毛羊膜炎の早期診断の指標)
D 癌胎児性フィブロネクチン(卵膜の損傷や脆弱化つまり破水の予知)
E 膣分泌物細菌培養(異常細菌の検出)
F 経膣超音波検査(外子宮口から内子宮口の長さの短縮傾向や内子宮口の開き具合)
G 胎児心拍陣痛モニタリング(胎児心拍の異常の有無と子宮収縮)
H 血液検査(白血球やCRPなど感染徴候のチェック)
I 経腹超音波検査(子宮内の羊水量測定、児の状態、血流測定)
(2) 「切迫早産」の治療
A 子宮収縮を抑制し、内診所見の進行を止めるため、子宮収縮抑制剤の投与を行う。
B 子宮内感染・絨毛羊膜炎の予防・治療として、膣内洗浄をする。
C 母体感染徴候がある場合、抗生物質の内服あるいは点滴投与を行う。
D 早産となる可能性が高い場合、週数によっては(34週未満)児の肺成熟を促す目的で、
副腎皮質ステロイドホルモンの筋肉注射を行う。
(3) 早産となる場合、週数によって児の予後はかなり変動する。したがって、分娩時期、方法は、
その時の児の状態や母体の状態により異なる。
A 妊娠22週~26週:児に後遺症(脳性麻痺の発症と関連する脳室周囲白質軟化症:PVLの
発生など)を生じる可能性が高く、新生児死亡の可能性もある。
B 妊娠27週~30週:児の生存に関しては予後良好な時期だが、上記後遺症を生じる場合も
ある。又、児の肺が未熟なため自立呼吸ができず、人工呼吸を必要とする場合が多くなる。
C 妊娠31週~34週:人工呼吸の必要性は個人差があるが、哺乳機能・免疫力・保温能力
などはまだ完全でない。
D 妊娠35週~36週:早産のため哺乳機能・免疫力・温能力などがまだ完全でない場合がある
ため、保育器管理が必要。
切迫早産の実際
切迫早産の予知
A 子宮頚管粘液中顆粒球エラスターゼ(エラスペック) 基準値1.6mg/ml以下 高値なら
2週間以内に早産となりリスクあり
B 癌胎児性フィブロネクチン(PTD)
胎児由来の糖蛋白質で、胎児血や羊水中に認められる。頚管粘液や膣分泌物中には通常
認められないが、細菌感染や子宮収縮による卵膜の損傷課程で膣内に流れ出してくる。
したがって、破水の診断や早産の予後因子として注目されている。
C 頚管因子
| 要注意所見 | 切迫早産 | ||
| 開大度 | 1cm~1.5cm | 2cm以上 | |
| 展退度 | 30%以上 | 50%以上 | |
| 頚管長 | 30mm以下 | 25mm以下 |

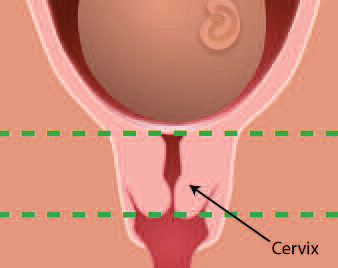
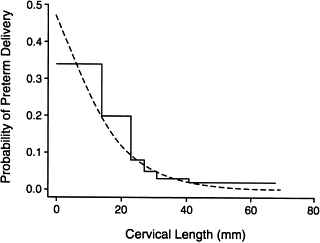 preterm before 35 wks ,cervical length at 24 wks
preterm before 35 wks ,cervical length at 24 wksurement.jpg)
Predicted probabilities of preterm delivery (PD)
before 37, 34, and 32 weeks according to first-trimester measurement
治療
(1)子宮収縮抑制剤
A 塩酸リトドリン(ウテメリン) b作動薬
・選択的b2刺激剤であるが、程度の差はあってもb1作用有する。
・経静脈投与(5%glucose + リトドリン1~3A(20~150mg))
初期投与50mg/分、 極量200mg/分
ウテメリン点滴方法
| 1A(50mg) | 2A(100mg) | 3A(150mg) | ||
| 50μg/分 | 30ml/hr | 15ml/hr | 10ml/hr | |
| 100μg/分 | 60ml/hr | 30ml/hr | 20ml/hr | |
| 150μg/分 | 90ml/hr | 45ml/hr | 30ml/hr | |
| 200μg/分 | 120ml/hr | 60ml/hr | 40ml/hr |
高血糖).肺水腫、無顆粒球症
B 硫酸マグネシウム(マグセント注100mL)
・経静脈点滴投与
1) loading
10%MgSO4 20ml(2g)を30分かけてDIVする(loading)
→40ml/hrを30分
2) keeping (10%MgSO4) 10ml(1g)/hr を点滴ポンプ
一般 0.4~1.0 g/hr(4~10ml/Hr)の速度で子宮収縮が抑制されるまで増量する。
通常最高20ml/Hr (2g/hr) までと言われている。
副作用:母体:中毒濃度(7mg/dl以上)を投与すると、呼吸抑制、テタニー、 心停止、
筋麻痺、低血圧、肺水腫
胎児: 胎児血中のMg濃度と母体血中濃度は相関する。そのため呼吸抑制による
代謝性アシドーシスと低カルシウム血症の代償機能障害に注意する。
#、マグネゾールを投与された児には脳障害が少ないとの報告がある。
C インドメタシン
PG合成酵素であるサイクロオキシゲナーゼの活性を抑制することにより子宮収縮は強く
抑制される。しかし、同時に胎児動脈幹を閉鎖し、胎児肺高血圧を誘起する可能性が指摘
され、日本では妊婦への投与は禁忌となっている(米国では使用)。
前期破水
前期破水について
前期破水(PROM:premature rupture of the membranes):
分娩開始前に卵膜の破綻をきたしたもの。
早期破水:分娩開始から子宮口全開大に至る以前に破水するもの。
preterm PROM:妊娠満37週未満での前期破水をいう。
当院における「前期破水」の管理について
(1) 「前期破水」の診断(補助診断も含む)
A 問診(破水を自覚した時期・量など)
B 内診(羊水流出の確認、卵膜の有無および子宮口の開きぐあい)
C BTB試験紙(青変))
C 子宮頚管粘液中顆粒球エラスターゼ(絨毛羊膜炎の早期診断の指標)
D 癌胎児性フィブロネクチン(卵膜の損傷や脆弱化つまり破水の予知)
E 羊水・膣分泌物細菌培養(異常細菌の検出)
F 経膣超音波検査(外子宮口から内子宮口の長さの短縮傾向や内子宮口の開き具合)
G 胎児心拍陣痛モニタリング(胎児心拍の異常の有無と子宮収縮)
H 血液検査(白血球やCRPなど感染徴候のチェック)
I 経腹超音波検査(子宮内の羊水量測定、児の状態、血流測定)
(2) 「前期破水」では、放置すると感染徴候が増悪したり、早産となることが危惧される。「1日でも
長く、子宮の中で児の成熟をはかりたい」そのために、次の内容を指標として児と母体の状態
を検討していく必要がある。
A 母体及び子宮内感染徴候のチェック:
母体発熱、血液検査(白血球やCRPの上昇)、子宮圧痛、胎児頻脈
B 経腹超音波:羊水量はどうか
C 経腹超音波:胎児は元気か、(成長障害、血流障害の有無)
D 胎児心拍モニタリング:胎児仮死徴候の有無(変動性一過性徐脈他)
(3) 「前期破水」の治療
A 子宮内感染・絨毛羊膜炎の予防:
抗生剤点滴(1st:マキシピーム→2nd:ペントシリン→ )
長くても5日で抗生剤は変更する。
GBS陽性例ではペントシリンがファーストチョイス
#以下の条件を満たすときはイセパシン筋注とする
1)母体及び子宮内感染徴候がない。
2)24時間以内に分娩となることが見込まれる。
3)細菌培養にて異常細菌が存在しない(特にGBS)
4)絨毛羊膜炎を合併していない
B 羊水流出の予防:バルーン留置、ベット上安静
しかし、よほどでなければ、排便はトイレで可能。できればバルーンも避けたい。
バルーン留置、ましてやベット上の排便は妊婦にとってすごいストレスです。実際、破水して
ても羊水は作られ続けており、トイレに立ったからといって羊水がなくなることはほとんど少ない。
それに、当院で管理する前期破水例は実際生まれても対応可能な症例のみである。
C 切迫早産の予防:切迫早産の項参照(子宮収縮抑制剤、膣洗浄等)
D 早期産となる可能性が高い、34週未満の症例:
副腎皮質ステロイドホルモン投与(別紙参照)
デカドロン 12mg 筋注(12時間後再投与)
搬送例は12mg1回、筋注し、紹介状にその旨を記載する。
(4) 管理方針
Preterm PROMは基本的に上記検査、治療、指標を参考に「1日でも長く児の成熟をはかる」
ことが目標である。 しかし、むやみに妊娠を継続し、感染等悪い状態で出生するなら、合併症
のない早産の方が相対的に児にとって負担が少ないといえます。よって、児の及び母体の状態
には常に気を配って観察する必要があります。また、37週以降の前期破水でも同じ事がいえ
ます。時間の経過とともに感染のリスクは上がっていきます。経膣分娩まで到達するか、常に
検討していく必要があります。
「前期破水の背景には絨毛羊膜炎や感染がすでに存在している可能性があることを十分認識
しておくことが大切です!!」
胎児肺成熟促進のためのステロイドホルモン投与 2001.10.12 森田
早産未熟児で出生するとどうなるのか?
最大の問題は呼吸機能が未成熟なため、呼吸不全へ進行する呼吸窮迫症候群(RDS)になることで
ある。 →RDSについては早産の弊害を参照
RDSを回避する方法はあるか?
早産の予防がもっとも効果的であり、医師は様々の治療により妊娠の継続を努力するわけである。
未熟児を生むことが避けられない妊婦に対しては、肺の成熟促進を目的とした
副腎皮質ステロイドホルモン投与が行われている。
ステロイドの効果、安全性は?
母体へステロイドを投与すると胎児へ移行して胎児の成熟を促し、早産児の死亡率、呼吸窮迫症候群、
脳室内出血を減少させることがわかっている。このステロイドの有益な効果は治療開始後24時間
以上経過した後に最大となるが、24時間未満でもその予後を改善させる。この治療法により新生児
あるいは母体への重大な副作用は認めておらず、また児の長期にも身体的発育や精神発達に
悪影響を及ぼさない事がわかっている。以上より、未熟児の分娩が予想される時、胎児の肺成熟を
目的としたステロイド投与は新生児の合併症軽減に有効と考える。
母体への副作用について
副作用としてアレルギー反応の伴うショック、感染症の報告があるが、希であり0.1%未満の発生と
いわれている。
ステロイドの投与方法は?
当院では早産が予期される妊娠34 週までの妊婦に対し,ベタメタゾン(リンデロン®)として1 回12mg を
24 時間ごとに計2 回,筋肉内注射する。ステロイドの効果は治療開始後7日間は継続するので、妊娠が7日間
以上維持できた場合は、必要に応じてステロイドを反復投与することがある。
【ベタメタゾン(リンデロン®)用法・用量】
(筋肉内注射)
通常,成人にはベタメタゾンとして1 回2~8mg を3~6 時間ごとに筋肉内注射する。
母体投与による新生児呼吸窮迫症候群の発症抑制に用いる場合,早産が予期される妊娠34 週までの妊婦に対し,
ベタメタゾンとして1 回12mg を24 時間ごとに計2 回,筋肉内注射する。
本剤投与から出産までの最適期間は投与開始後24 時間以上7 日間以内である。また,それ以降に本剤を繰り返し
投与した際の有効性と安全性は確立されていないので,児の娩出時期を考慮して投与時期を決定すること。
注) 早産児の弊害
早産は全分娩の約5%に認められ、周産期の罹患率と死亡率の最大原因を占めている。未熟児の
合併症として呼吸窮迫症候群、脳室内出血、壊死性腸炎、気管肺低形成、動脈幹開存、敗血症、
網膜症等があげられるが、特に呼吸窮迫症候群は早期産児の予後を左右することから今日なお
未熟児医療において重要な位置をしめている。呼吸窮迫症候群は(RDS)とは進行性呼吸不全を
呈する未熟児の代表的疾患であり、在胎周数が少ないほど、体重が小さいほど発症頻度が高くなる。
原因は肺未成熟にともなう肺表面活性物質(肺サーファクタント)の欠乏が主因だが、人工換気療法と
人工肺サーファクタント補充療法の導入により、治療は飛躍的な進歩を遂げている。しかし治療に
用いられる高濃度の酸素や長期にわたる人工換気などが原因となる慢性肺疾患が問題となるなど、
RDSは現在も未熟児医療における大きな問題である。
当院ではこれらの治療を行って、元気な赤ちゃんが生まれてくるように努めています。